 返回
分享
返回
分享
化妆品FDA注册怎么收费?公司注册和产品注册有什么区别?
 2024-11-06 10:43:02
2024-11-06 10:43:02
FDA《商品包装和标签法》的颁布其实就是对化妆品标签的严格而明确的规定。在市场上销售的化妆品都必须要符合这个规定的,因为这是评价化妆品合格与否的主要依据,也是管理化妆品的主要内容,标签不符合要求的化妆品禁止市售,这里小编将FDA化妆品标签要求整理如下。
化妆品FDA标签的基本信息:
1.标签:
本术语是指产品上的所有标签和其他书面、印刷或图形材料(FD&C法案,SEC),201(M);21 U.S.C.321(M)]。
2.主要展示面板(Pdp):
这是标签中最有可能展示或检查的部分,在通常的展示条件下出售[21 CFR 701.10]。
3.信息面板:
通常,这个术语指的是PDP以外的面板,它可以容纳消费者可能看到的标签信息,这个面板上的信息必须是突出和显眼的。
举列:
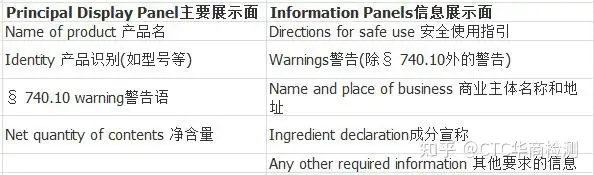
作为禁止虚假或误导性信息的一部分,任何化妆品都不能被贴上标签或用声明表明FDA已经批准了该产品。即使制造机构已注册,或产品已提交FDA存档,也是如此。自愿化妆品注册计划所有美国法律或法规要求的标签信息都必须是英文的。
这条规则的唯一例外是只在一种不同语言占主导地位的美国领土上销售的产品,例如波多黎各。如果化妆品的标签包含任何外国语言的表示,所有根据FD&C法案所要求的标签信息也必须以该语言出现[21 CFR 701.2(B)]。
标签FDA认证要求
1、标签:这个术语是指产品或附带的所有标签和其他书面、打印或图形的内容[FD&C Act,sec,201(m);
21USC321(m)]。
2、主要显示面板(PDP):是在展示销售条件下经常展示或检验的标签的一部分[21 CFR 701.10]。
3、信息面板:通常,这个术语指的是非PDP面板,可以容纳消费者可以看到的标签信,因此通常不能用于在包装底部放置化妆品成分声明等必要信息。
是否允许化妆品“FDA批准”的标记
不,作为禁止虚假或误解的信息的一部分,任何化妆品不得贴标签或做广告。如果FDA宣布批准产品,企业注册或产品参照FDA自主化妆品注册计划(VCRP)(21CFR710.8和720.9),禁止加入VCRP并得到正式批准,也适用。
产品既是药品又是化妆品时,应该如何贴标签
产品为非处方药(OTC)和化妆品时,其标签必须符合OTC药物和化妆品成分标签的规定(21CFR701.3)d),药物成分为OTC药物标签的要求)21CFR201.66)。
化妆品的强制标签要求
主显示器上必须显示以下信息:
1、身份证以公共或常规名称、说明性名称、公众可理解的幻想名称或插图[21 CFR 701.11]来表示产品的性质和用途;
2、通过重量、尺度、数字计数或数字计数与重量或尺度的组合,准确说明净含量[21 CFR 701.13];
3、名称和营业所;
4、经销商声明;
5、警告和警告声明;
6、成分、这些必需标签所要求的显示方式和位置因标签的大小和销售方法而异。

部分过审案例






